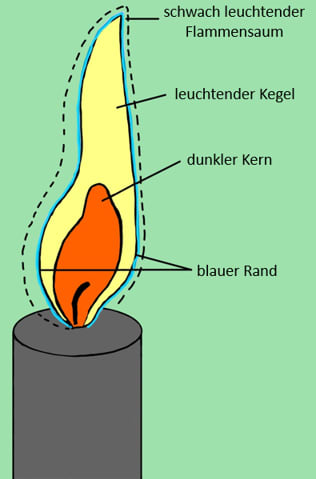
Unter Leuchterscheinungen und Hitzeentwicklung brennende Gase bzw. Dämpfe. Mit Flammen verbrennen alle brennbaren Gase sowie solche Flüssigkeiten und Feststoffe, die oberhalb ihrer Entzündungstemperatur brennbare Dämpfe bzw. brennbare dampfförmige Zersetzungsprodukte entwickeln. Gewöhnlich sind an der Flammenbildung zwei Reaktionspartner beteiligt, ein Brennstoff und ein Oxidationsmittel. Bei den Oxidationen kommt es zu Kettenreaktionen von Radikalen. Die Wirkung von Feuerlöschmitteln beruht u. a. darauf, dass sie Radikale wegfangen. Streng genommen beschränkt sich der Begriff Flamme auf die Reaktionszone. Üblicherweise werden zur Flamme aber auch noch andere gasförmige Bereiche gezählt, nämlich diejenigen, die von der Reaktionszone umschlossen werden oder diese von außen umgeben, und zwar dann, wenn sie leuchten oder wenn in ihnen noch in geringem Umfang Reaktionen ablaufen. So besteht z. B. eine ruhig brennende Kerzenflamme (siehe Abb.) aus drei einander umhüllenden Zonen.
Die innere Zone, der dunkle Kern, wird hauptsächlich aus den durch thermische Zersetzung des Kerzenmaterials entstandenen gasförmigen Kohlenwasserstoffen gebildet; diese verbrennen hier nicht, da der dazu nötige Sauerstoff fehlt; die Temperatur liegt zwischen 300 und 520 °C.
Die vollständige Verbrennung der Kohlenwasserstoffe zu Kohlenstoffdioxid und Wasser erfolgt im nahezu unsichtbaren Flammensaum, dem Außenmantel, da hier genügend Sauerstoff vorhanden ist. In dieser Zone, dem heißesten Bereich der Flamme, wird eine Temperatur von bis zu 1100 °C erreicht. In der mittleren Zone, dem gelb leuchtenden Kegel, herrscht Sauerstoffmangel, sodass hier nur eine unvollkommene Verbrennung stattfinden kann, die gasförmigen Kohlenwasserstoffe werden hier zersetzt, wobei auch freier Kohlenstoff entsteht. Die festen Kohlenstoffteilchen werden so stark erhitzt, dass sie glühen und somit das Leuchten der Flamme verursachen. Die Kerzenflamme sowie die leuchtende Flamme des Gasbrenners (Brenner) zählen zu den Diffusionsflammen, bei denen Brennstoff und Oxidationsmittel erst in der Reaktionszone vermischt werden. Die schwach leuchtende Brennerflamme ist hingegen eine vorgemischte Flamme, bei der ein homogenes Brennstoff-Luft-Gemisch verbrennt. Stark leuchtende Flammen, die den von ihnen benötigten Sauerstoff sauerstoffhaltigen Verbindungen entziehen, diese also reduzieren können, werden Reduktionsflammen genannt. Umgekehrt bezeichnet man sauerstoffreiche Flammen, wie z. B. die schwach leuchtende Bunsenbrennerflamme, als Oxidationsflammen. In Oxidationsflammen werden Temperaturen von 1300–2000 °C erreicht, in Reduktionsflammen von 1000–1100 °C.