Der „Atomkern“ oder kurz „Kern“ ist der nur etwa 10–15 m (1 fm, dies ist weniger als ein Zehntausendstel des Atomdurchmessers) große Zentralbereich eines Atoms. In diesem ist die gesamte positive Ladung und fast die gesamte Masse konzentriert, (die Massendichte von Kernmaterie beträgt etwa \(1,4\cdot 10^{17}\,\text{kg/m}^3\).
Atomkerne enthalten Protonen und Neutronen, die man zusammengenommen auch Nukleonen (von lat. nucleus „Kern“) nennt. Die Zahl A der Nukleonen im Kern ist die Massenzahl, die Zahl der Protonen die Ordnungszahl Z und die Zahl der Neutronen die Neutronenzahl N. Offensichtlich ist A = Z + N. Da die Protonenzahl das chemische Element bestimmt, zu welchem ein Kern gehört, beschreibt man Kerne nach dem Schema:
\(^A_Z\text{Elem.}_N\) oder kurz AElem. bzw. Elem.-A
also z. B. für den leichten Wasserstoffkern \(^1_1\text H_0\), 1H oder H-1 und für den Urankern mit 146 Neutronen \(^{238}_{\ \ 92}\text U_{146}\), 238U oder U-238. Atomkerne mit gleicher Protonen- und unterschiedlicher Neutronenzahl heißen Isotope.
Nach dem sog. Tröpfchenmodell des Atomkerns ähnelt dieser einer Flüssigkeit, in der die Nukleonen dicht an dicht, aber gegeneinander beweglich gebunden sind. Die Anziehungskraft beruht dabei in erster Linie auf der ganz abgeschirmten starken Wechselwirkung bzw. Farbkraft zwischen den Quarks in den Nukleonen, die man in diesem Zusammenhang meist Kernkraft nennt. Dem wirkt die schwächere elektrostatische Abstoßung zwischen den Protonen entgegen, eine Art Oberflächenspannung sowie bestimmte quantenmechanische Effekte spielen ebenfalls eine Rolle. Mit dem Tröpfchenmodell lässt sich z. B. die Abhängigkeit der Kernbindungsenergie von der Massenzahl beschreiben (s. u.).
In einem anderen Kernmodell, dem Schalenmodell, werden für Protonen und Neutronen wie für die Elektronen in der Atomhülle Orbitale berechnet, die mit geeigneten Quantenzahlen durchnummeriert werden. Dieses Modell sagt bestimmte besonders stabile Atomkerne voraus, bei denen wie in einer Edelgaskonfiguration abgeschlossene Schalen für Protonen oder Neutronen vorliegen. Die entsprechenden Protonen- und Neutronenzahlen nennt man magische Zahlen. Am stabilsten sind doppeltmagische Kerne wie das Alphateilchen 4He und die Kerne 16O und 208Pb.
Die Bindungsenergie eines Kerns beträgt pro Nukleon einige MeV, dies ist ein messbarer Bruchteil der Ruheenergie eines Nukleons (knapp 1000 MeV). Aufgrund der Äquivalenz von Masse und Energie ist die Masse eines Atomkerns gerade um diese Energiemenge (geteilt durch c2) kleiner als die Massensumme seiner Nukleonen, dies nennt man den Massendefekt.
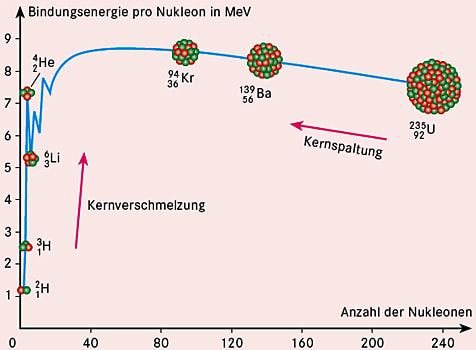
Die Bindungsenergie pro Nukleon ist bei mittelschweren Kerne mit \(A \approx 60\) am größten, sie nimmt zu leichteren und schwereren Kernen hin ab, bei den leichtesten Kernen ist sie am schwächsten. Daher kann man durch die Spaltung schwerer Kerne Energie gewinnen, bei der Fusion leichter Kerne sogar noch mehr.
Nicht alle Kerne sind stabil. Instabile Kerne gehen mit einer gewissen Wahrscheinlichkeit in andere Kerne über, wobei Energie in Form von Teilchen- und elektromagnetischer Strahlung frei wird.